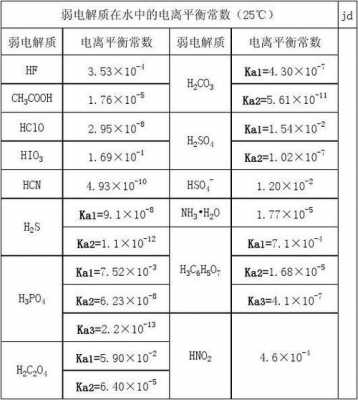
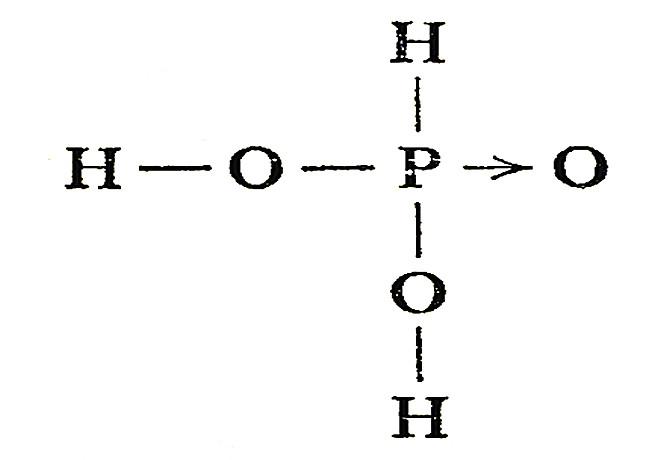
磷酸的电离平衡常数 磷酸盐电离平衡常数
欢迎进入本站!本篇文章将分享磷酸盐电离平衡常数,总结了几点有关磷酸的电离平衡常数的解释说明,让我们继续往下看吧!
琥珀酸的电离平衡常数
1、H2PO4-的电离常数为bai2*10-8,水解常du数zhi为Kw/K1=33*10-12,电离大於水解所以dao是酸性。HPO42-的电离常数为zhuan2*10-13,水解常数为Kw/K2=61*10-7,水解大於电离所shu以是碱性。
2、酸度系数=pKa酸度系数,又名酸离解常数,代号Ka值,在化学及生物化学中,是指一个特定的平衡常数,以代表一种酸离解氢离子的能力。该平衡状况是指由一种酸(HA)中,将氢离子(即一粒质子)转移至水(H2O)。
3、分析化学书上有个图:草酸氢钠和草酸钠和草酸在PH=3左右,交叉严重,说明此时溶液中成分比较复杂,导致这个原因就是草酸Ka1=5.9*10^-2,Ka2=10^-5。两个电离常数级别相差不太大,所以不能准确被滴定到草酸氢钠。
4、设缓冲系统的弱酸的电离常数为K(平衡常数),平衡时弱酸的浓度为[酸],弱酸盐的浓度为[盐],则由弱酸的电离平衡式可得下式:PH=PK-lgc酸/c盐。
今有一磷酸盐溶液的pH=9.78,其主要存在形式是已知H3PO4的解离常数PKa1...
当pH大于167时,其主要存在形式是PO。
H3PO4是三元酸。H3PO4是磷酸的化学式,磷酸是三元中强酸,分三步电离,不易挥发,不易分解,有一定氧化性。具有酸的通性。
实际上,磷酸是中强酸,其解离是可逆的,在一定条件下有一定的解离常数(用Ka表示)。计算PH要依据解离常数。
密度:685g/ml (液体状态)熔点:435 ℃(316K)沸点:158℃(431 K)(分解,磷酸受热逐渐脱水,因此没有自身的沸点)市售磷酸是含85%H3PO4的粘稠状浓溶液。
得到NaH2PO4;pH=1/2(pKa1+pKa2)。
磷酸根在水中会发生水解,产物分别是HPO4(2-),H2PO4(-),以及H3PO4。应该是PO4(3-),HPO4(2-),H2PO4(-),以及H3PO4同时存在。
饲料级磷酸盐/是什么东西,包括什么?
问题一:磷酸盐是什么 “磷酸盐”是“磷的含氧酸盐”的通称,磷酸盐可以 分为简单磷酸盐和复杂磷酸盐两类。简单磷酸盐是指 正磷酸的各种盐类,如M3POM2HPO4和MH2PO4(M为一 加金属离子,如磷酸二氢钾)。
“磷酸盐”是“磷的含氧酸盐”的通称。磷酸盐可以分为简单磷酸盐和复杂磷酸盐两类。简单磷酸盐是指正磷酸的各种盐类,如M3POM2HPO4和MH2PO4(M为一加金属离子,如磷酸二氢钾)。
食品:磷酸是食品添加剂之一,在食品中作为酸味剂、酵母营养剂,可乐中就含有磷酸。磷酸盐也是重要的食品添加剂,可作为营养增强剂。医学:磷酸可用于制取含磷药物,例如甘油磷酸钠等。
在农业上,磷酸盐是植物的三种主要养分之一,且是肥料的主要成份。磷矿粉是从沉积岩的磷层中开采。以前它在开采后不用加工便可使用,但现时未加工的磷酸盐只会用在有机耕种上。
各种pH的缓冲溶液怎么配制
乙醇-醋酸铵缓冲液(pH7):取5mol/L醋酸溶液10ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至7,用水稀释至1000ml。
.1 mol/LHCl:量取1ml浓盐酸(12mol/L)溶于119ml蒸馏水中制成。将以上两种溶液按以上比例混合均匀后,加蒸馏水定容到100ml即可。
(4)硼砂标准缓冲液精密称取硼砂 81g(注意避免风化),加水使溶解并稀释至1000ml,置聚乙烯塑料瓶中,密塞,避免空气中二氧化碳进入。
缓冲溶液的配制方法如下:根据所需求的酸碱性选择合适的缓冲对,若是配制酸性缓冲液就选择弱酸与弱酸盐缓冲对;若是配制碱性缓冲液就选择弱碱与弱碱盐缓冲对。
配制方法:只要知道缓冲对的PH值,和要配制的缓冲液的pH值(及要求的缓冲液总浓度),就能按公式计算[盐]和[酸]的量。
磷酸的三步电离平衡常数
1、pH=7时,主要是H2PO4(-)和HPO4(2-),且后者据多。将磷酸的各级酸根离子处理成共轭酸碱,即:共轭酸H3PO4——共轭碱H2PO4(-)对应Ka1。共轭酸H2PO4(-)——共轭碱HPO4(2-)对应Ka2。
2、如果K2,K3电离常数是由磷酸盐电离测出的,这种说法就明显是错的。一般来说,这类多元酸各级电离程度都是递减的,原因与分子以及离子间的作用力,你可以简单理解成越调皮的孩子跑出去的越快。
3、或者是可以给出质子(氢离子)的物质。碱:电离时能吸收质子的物质为碱性,阴离子全为OH-的为碱类。盐:酸与碱中和的产物(中和反应),由金属离子(包括铵根离子)与酸根离子构成。
4、增大 K值越大,酸性越强 这个得看电离常数,电离常数越大,酸性越强。
磷酸的化学性质
磷酸是三元中强酸,分三步电离,不易挥发,不易分解,几乎没有氧化性。具有酸的通性。
物理性质:纯净的磷酸是无色晶体,高沸点酸,易溶于水。市场销售的磷酸试剂是粘稠的、不挥发的浓溶液,磷酸含量为百分之八十三到百分之九十八。
磷酸,分子式为:H3PO4,是一种常见的无机酸。易溶于水 各种磷酸根离子跟硝酸银反应生成的沉淀颜色不同,在硝酸中的溶解性不同,酸化后跟蛋白溶液的作用也不同。利用这些性质可以鉴别各种磷酸根离子。
小伙伴们,上文介绍磷酸盐电离平衡常数的内容,你了解清楚吗?希望对你有所帮助,任何问题可以给我留言,让我们下期再见吧。