磷酸盐的溶解性有什么规律
各位访客大家好!今天小编关注到一个比较有意思的话题,就是关于磷酸盐溶解分析法的问题,于是小编就整理了几个相关介绍的解答,让我们一起看看吧,希望对你有帮助
关于磷酸盐的溶解
1、加入盐酸:CaHPO+2HCl=CaCl+HPO(沉淀溶解)【如果盐酸不足量,也会产生磷酸二氢钙和氯化钙部分溶解。2CaHPO+2HCl=CaCl+Ca(HPO)】。
2、钾、钠、铵盐都可溶,即磷酸钾、磷酸钠、磷酸铵可溶。磷酸钾、磷酸钠、磷酸铵是正盐,磷酸一氢钾(K2HPO4)、磷酸一氢钠(Na2HPO4)是磷酸一氢盐,磷酸二氢钾(KH2PO4)、磷酸二氢钠(NaH2PO4)是磷酸二氢盐。
3、一氢、二氢和正盐:K+,Na+,NH4+都易溶,碱金属除Li外磷酸盐均易溶于水。难溶正盐:Ag+,Ca2+,Mg2+,Sr2+,Ba2+,Bi3+,Fe3+,NH4MgPO4,Ni2+,Pb2+,Zn2+等,大部分金属离子都难溶。
4、磷酸盐可以溶于水而不溶于乙醇、乙酸乙酯、丙酮、二氯乙烷、二氯异氰尿酸钠等有机溶剂中,也可以溶于苯、三氯乙烷、氯仿、乙二醇等有机溶剂中。
5、磷酸盐溶解度大体关系:磷酸二氢盐磷酸一氢盐磷酸正盐。所有的磷酸二氢盐都可溶。磷酸一氢盐,磷酸正盐:钾钠铵均可溶(也包括Rb+和Cs+),其余盐都不溶(包括Li+)。
磷酸盐哪些可溶,哪些不可溶
1、磷酸盐和磷酸一氢盐除K+、Na+、NH4+盐外,一般都不溶于水。
2、钾、钠、铵盐都可溶,即磷酸钾、磷酸钠、磷酸铵可溶。磷酸钾、磷酸钠、磷酸铵是正盐,磷酸一氢钾(K2HPO4)、磷酸一氢钠(Na2HPO4)是磷酸一氢盐,磷酸二氢钾(KH2PO4)、磷酸二氢钠(NaH2PO4)是磷酸二氢盐。
3、磷酸的钠、钾、铵盐及磷酸的二氢盐都易溶于水!而磷酸的一氢盐和正盐,除钠、钾、铵盐以外,一般都难溶于水。
4、磷酸的所有二酸式盐(磷酸二氢盐)都易溶于水,而一酸式盐(磷酸氢盐)和磷酸正盐(钠、钾、铵的盐外),一般不溶于水。
5、磷酸铜,蓝色斜方系晶体,溶于氨水,稀酸和铵盐溶液中。不溶于水和液氨中!磷酸镁,白色正交系晶体,溶于氨水和稀酸溶液。不溶于水和液氨!磷酸铁的固体为白色粉末不溶于水和醋酸,溶于稀酸。磷酸一氢铁。
请问磷酸盐的溶解性有什么规律?
加入盐酸:CaHPO+2HCl=CaCl+HPO(沉淀溶解)【如果盐酸不足量,也会产生磷酸二氢钙和氯化钙部分溶解。2CaHPO+2HCl=CaCl+Ca(HPO)】。
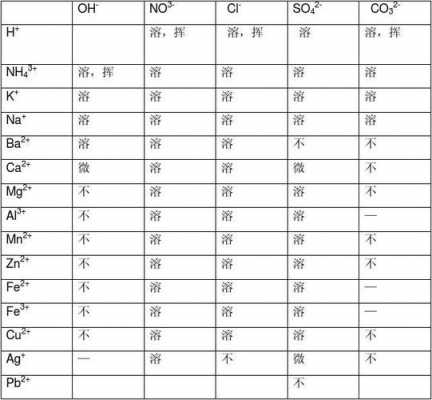
钾钠铵硝皆可溶,氯盐不溶银亚汞;硫酸盐不溶钡和铅,碳磷酸盐多不溶。多数酸溶碱少溶,只有钾钠铵钡溶。口诀四:钾、钠、硝酸溶,钾盐、钠盐和硝酸盐都溶于水。
钾钠铵硝皆可溶、盐酸不溶银亚汞。硫酸不溶钡和铅、碳磷酸盐多不溶。多数酸溶碱少溶、只有钾钠铵钡钙。钾钠铵盐硝酸盐,完全溶解不困难。氯化亚汞氯化银,硫酸钡和硫酸铅。生成沉淀记心间,氢硫酸盐和碱类。
一氢、二氢和正盐:K+,Na+,NH4+都易溶,碱金属除Li外磷酸盐均易溶于水。难溶正盐:Ag+,Ca2+,Mg2+,Sr2+,Ba2+,Bi3+,Fe3+,NH4MgPO4,Ni2+,Pb2+,Zn2+等,大部分金属离子都难溶。
磷酸盐,磷酸一氢盐,磷酸二氢盐的溶解性如何?
1、一氢、二氢和正盐:K+,Na+,NH4+都易溶,碱金属除Li外磷酸盐均易溶于水。难溶正盐:Ag+,Ca2+,Mg2+,Sr2+,Ba2+,Bi3+,Fe3+,NH4MgPO4,Ni2+,Pb2+,Zn2+等,大部分金属离子都难溶。
2、磷酸的所有二酸式盐(磷酸二氢盐)都易溶于水,而一酸式盐(磷酸氢盐)和磷酸正盐(钠、钾、铵的盐外),一般不溶于水。
3、其余不溶;氯化物除氯化银不溶,其余全溶;碳酸盐、硅酸盐、硫化物除钾、钠、铵溶外,其余一般不溶;酸式盐一般都溶,但磷酸盐特殊:磷酸二氢盐全溶,磷酸盐、磷酸一氢盐除钾、钠、铵外,其余一般不溶。
4、一般除钠钾铵盐磷酸一氢盐不溶于水磷酸二氢盐都易溶于水。至于其他溶剂高考不做要求。
5、磷酸铜,蓝色斜方系晶体,溶于氨水,稀酸和铵盐溶液中。不溶于水和液氨中!磷酸镁,白色正交系晶体,溶于氨水和稀酸溶液。不溶于水和液氨!磷酸铁的固体为白色粉末不溶于水和醋酸,溶于稀酸。磷酸一氢铁。
熔融分解法中,为什么氢氧化钠能用来熔融分解磷酸盐,怎么反应的?(按理...
1、浓磷酸可以和氯化钠共热生成氯化氢气体(与碘化钾、溴化钠等也有类似反应),属于高沸点酸制低沸点酸。磷酸受强热时脱水,依次生成多聚磷酸,焦磷酸、三磷酸和多聚的偏磷酸。三磷酸是链状结构,多聚的偏磷酸是环状结构。
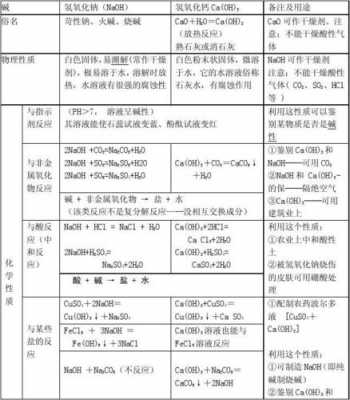
2、溶解性:极易溶于水,溶解时放出大量的热。易溶于乙醇、甘油。化学性质 碱性 氢氧化钠溶于水中会完全解离成钠离子与氢氧根离子,所以它具有碱的通性。
3、氢氧化钠受热分解如下:会融化,熔融状态下,变成离子状态,即氢氧化钠分子变成了钠离子和氢氧根离子,放置久了会变成碳酸钠。
4、熔化:熔化是通过对物质加热,使物质从固态变成液态的变化过程。熔化要吸收热量,是 吸热过程 。溶解:广义上说,超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解。
5、Na元素与水反应(与水反应时,应用烧杯并在烧杯上加盖玻璃片,反应时钠块浮在水面上,熔呈球状,游于水面,有“嘶嘶”的响声,并有生成物飞溅),生成强碱性NaOH溶液,并放出氢气。
6、原理:2NaOH + CO2=== Na2CO3+ H2O2HCl + Na2CO3=== 2NaCl + CO2↑+ H2O(空气中含有少量的二氧化碳,而敞口放置的NaOH溶液能够与CO2反应HCl中的氢离子能够与碳酸根离子反应生成气体)注:HCl会优先与NaOH反应生成NaCl和H2O。
小伙伴们,上文介绍磷酸盐溶解分析法的内容,你了解清楚吗?希望对你有所帮助,任何问题可以给我留言,让我们下期再见吧。